VNS
VAGAL SİNİR STİMÜLASYONU VE HASTA SEÇİMİ
Semai BEK(1), Ersin ERDOĞAN(2), Zeki GÖKÇİL(1)
(1) GATA Tıp Fakültesi Nöroloji AD Ankara
(2) Ufuk Üniversitesi Tıp Fakültesi Beyin ve Sinir Cerrahisi AD Ankara
Onay almış tek stimülasyon tekniği olan vagal sinir stimülasyonu (VSS) ilk kez 1988 yılında bir hasta üzerinde denenmiştir. 1989 yılında Amerikan Epilepsi Derneği toplantısında olgu sunumu olarak bildirilen bu hastaya ait başarılı sonuçlar bir yıl sonra yayımlanarak bilim dünyası ile paylaşılmıştır
(1). Bu sunumu takiben planlanan ve yürütülen beş klinik çalışmanın daha hepsi sonuçlanmadan VSS, 1994 yılında Avrupa Birliği ve 1997 yılında ise Amerikan Gıda ve İlaç Dairesi (Food and Drug Administration – FDA) tarafından epilepsi hastalarında kullanılmak üzere onay almıştır. Sekonder jeneralizasyon görülsün veya görülmesin parsiyel başlangıçlı, 12 yaş üstü tedaviye dirençli epilepsi hastalarında nöbet sıklığının azaltılması amacıyla ek tedavi olarak onay alan VSS, bu tarihten sonra yaygın olarak kullanıma girmiştir.
Sonraki yıllar içerisinde VSS konusundaki deneyimler arttıkça FDA’nın onay şartları eleştiri konusu olmuş ve bu şartların daha da esnetilmesi konusunda itirazlar olmuştur. 1999 yılında Amerikan Nöroloji Akademisi ise bu şartlara ek olarak bir de rezektif cerrahi adayı olamayacak hastalarda kullanılması gerektiğini belirterek VSS kullanımını daha da sınırlandırmıştır. 2000 yılında yaklaşık 3000 hastaya VSS takıldığı bilinmektedir. 2010 yılında ise bu sayının 60000’in üstünde olduğu kabul edilmektedir. Bu kadar kısa süre içerisinde, bu kadar kısıtlamaya rağmen yine de yaygın bir şekilde kullanıma giren VSS’e ait sonuçlar 2011 yılında bir meta-analizde sunulmuştur
(2). Toplam 74 klinik çalışmanın değerlendirildiği ve 3321 hastanın klinik verilerinin analiz edildiği bu yazıya göre VSS sanıldığının aksine son seçenek değil ama tedaviye dirençli epilepsi hastalarında gerçek anlamda bir ek tedavi modalitesi olarak sunulmaktadır.
Net etki mekanizması hala bilinmemekle beraber sinaptik aktivite üzerine etkili olduğu düşünülmektedir. Mekanizmayı anlamaya yönelik tüm çalışma ve uygulamalar hayvan deneylerine dayanmaktadır. Talamus, talamokortikal projeksiyonlar, hipotalamus ve insulada sinaptik aktivitenin artarak, ayrıca hipokampus ve amigdalada da sinaptik aktivitenin azalarak kortikal Nöronal senkronizasyonda azalmanın sağlandığı hipotezi hakimdir. Bunun sonucunda interiktal ve iktal aktivitede azalma sağlanmakta, uyanıklık artmakta (özellikle serebral palsili hastalarda nöbet sıklığında azalmaya ilaveten ikincil etki olarak değerlendirilmektedir) ve norepinefrin ve serotonin salınımı artmaktadır (muhtemelen depresyon tedavisindeki etki mekanizması da bu yola dayandırılmaktadır).
Hemen hepsi geri dönüşlü olup, birçoğu yalnızca stimülasyon sırasında gözlenen ve hemen hemen hiçbir zaman tedavinin sonlanmasına neden olabilecek kadar şiddetli olmayan yan etkiler arasında ses kabalaşması, çenede uyuşma, öksürük, boğaz ağrısı, dispne, dispepsi, disfaji, baş ağrısı ve kardiak ritm bozukluğu sayılabilir. Çalışma sonuçları değerlendirilirken epilepsi cerrahisi sonuç değerlendirmesinde yaygın olarak kullanılan Engel veya modifiye Engel sınıflandırmaları kullanılmıştır (Tablo 1 ve 2). 2007 yılında ise yalnızca VSS sonrası kullanılabilecek ve özellikle hastanın magnet uyarımı ile kendisi tarafından durdurulan nöbetlerin de sınıflandırmaya alındığı McHugh sınıflandırması teklif edilmiştir
(3). Bu sınıflandırma Engel sınıflandırmasına göre çok daha sade olması ve magnet uyarımını da içermesi nedeniyle bu tarihten sonra yayımlanan çalışmalarda kullanılmıştır (Tablo 3).
Mekanizması hala hipotetik olan bu tedavi modalitesinin kullanıldığı tüm çalışmalarda birincil sonlanım noktası olarak nöbet sıklığında azalma kriter olarak alınmıştır. Kullanılan antiepileptik ilaçların (AEİ) azaltılması veya yaşam kalitesindeki artış ise bazı çalışmalarda ikincil sonlanım noktası olarak değerlendirilmiştir.
| Klas I | Özürlülük oluşturan nöbet yok |
A | Cerrahi sonrası tam nöbetsizlik |
B | Özürlülük oluşturmayan yalnızca basit parsiyel nöbetler |
C | Cerrahi sonrası özürlülük oluşturan bazı nöbetler ancak son iki yıldır özürlülük oluşturan nöbetlerin hiç olmaması |
D | Yalnızca ilaç kesimi sonrası jeneralize konvülsiyon |
Klas II | Özürlülük oluşturan nöbet nadir |
A | İlk dönem özürlülük oluşturan nöbet hiç olmamasına rağmen son dönemde nadiren olması |
B | Cerrahiden bu yana nadiren özürlülük oluşturan nöbetlerin bulunması |
C | Cerrahiden beri olan özürlülük oluşturan nöbetlerin son iki yılda nadir olması |
D | Yalnızca nokturnal nöbetler |
Klas III | Kayda değer gelişme |
A | Nöbet sıklığında kayda değer azalma |
B | Nöbetsiz dönemlerin uzaması (ancak iki yıldan daha az) |
Klas IV | Kayda değer gelişme yok |
A | Nöbet sıklığında belirgin azalma |
B | Nöbet sıklığında belirgin değişiklik yok |
C | Nöbet sıklığında artış veya nöbetlerde kötüleşme |
Tablo 1: Engel sınıflaması
2011 yılında yayımlanan ve 74 klinik çalışmanın değerlendirildiği bu meta-analizin sonuçlarına baktığımızda yaklaşık olarak hastaların %50’sinde nöbet sıklığında >%50 azalma, %24’ünde nöbet sıklığında <%50 azalma, %24’ünde nöbet sıklığında azalma olmadığı (veya artış olduğu) saptanmıştır. Farklı çalışmalarda değişik sonuçlar bildirilmekle beraber tam nöbetsizlik oranı en fazla %5 olup ortalama %2 olarak görülmektedir.
Takip sürelerine göre nöbet sıklığındaki değişimler değerlendirildiğinde ise takip sürelerinin artması ile nöbet sıklığında azalma arasında doğrusal bir korelasyon görülmektedir. Cerrahi sonrası 3 – 12 ay arası nöbet sıklığında %50 azalmanın sağlandığı olgular %36,2 iken bu oran 12. aydan sonra %51’e çıkmaktadır. Eliot ve ark.nın tedaviye dirençli 65 hastanın VSS sonuçlarını 10 yıldan fazla süre takip ettikleri çalışmanın sonuçları da yine takip süresi arttıkça nöbet sıklığında azalma olan hastaların oranlarının arttığı sonucu ile uyumludur (4). Bu çalışmada her geçen yıl nöbet sıklığında azalma olan hastaları oranlarının arttığı gösterilmekle beraber bu artışın ikinci yıldan sonra anlamlı olmadığı ifade edilmiştir. Bu sonucu tersten değerlendirirsek VSS cerrahisi sonrası sonuçları değerlendirebilmek için ikinci yılsonu takip sonuçlarını beklememiz gerektiği sonucunu da çıkarabiliriz.
Klas I | Nöbet yok, nadir, özürlülük oluşturmayan basit parsiyel nöbetler |
KIas II | Nöbet sıklığında >%90 azalma, nadiren kompleks parsiyel nöbetler |
Klas III | Nöbet sıklığında %50-90 azalma |
Klas IV | Nöbet sıklığında <%50 azalma |
Tablo 2: Modifiye Engel Sınıflaması
Uzun süreli takipte sonuçların daha başarılı olması net olarak açıklanamamaktadır ancak etki mekanizması bile tam olarak anlaşılamamasına rağmen VSS’nin bir kümülatif etkisinin olabileceği üzerinde durulmaktadır. Buna ilaveten hastaların iki yıl gibi bir süre içerisinde AEİ’lerinin ancak düzenlenebilmesi de bu sonuca katkıda bulunuyor olabilir.
Uygulama yaşı ise başlıca bir tartışma konusudur. Daha önce belirttiğimiz gibi FDA onayı 12 yaş üstü hastalara verilmiş olmasına rağmen çalışma sonuçları bu sınırın esnetilmesi gerektiğini göstermektedir. 18 yaş üstü hastaların %49,5’inde >%50 nöbet sıklığında azalma olmasına karşın bu oran 18 yaşın altında %55,3’e, hatta 6 yaşın altında %62’ye çıkmaktadır. Bazı çalışmalarda hasta yaşının 1 yaşına kadar aşağıya çekilmiş olması da dikkat çekicidir (5-7).
Nöbet tipi açısından değerlendirildiğinde sanılanın aksine jeneralize epilepsilerde nöbet sıklığında %57,5 azalma gözlenirken parsiyel epilepsilerde %42,5 nöbet sıklığında azalma gözlenmiştir. Karışık tip nöbeti olan hastalarda ise nöbet sıklığında azalma oranı %53,7’dir. Bu sonuç, akıl karıştırıcı gibi görünmekle beraber buradaki parsiyel epilepsi hastalarının rezektif cerrahi adayı olamayan nispeten komplike olgulardan oluştuğu unutulmamalıdır. Parsiyel başlangıçlı epilepsilerin frontal lob ve temporal lob kaynaklı olmasına göre ayrıldığı bir çalışmada ise %50’den fazla nöbet sıklığında azalmanın frontal lob epilepsi hastalarının %65’inde ve temporal lob epilepsi hastalarının %15’inde sağlandığı gösterilmiştir (8). Yine başka bir çalışmada VSS’nin etkinliğinin psikomotor nöbetlerde daha az olduğu gösterilmiştir (9). Ayrıca interiktal epileptiform deşarjları (İED) unilateral olgularda nöbet sıklığında azalmanın daha yüksek oranda olduğu da bu çalışmada belirtilmiştir. Pediatrik yaş grubunda yapılan çalışmada ise VSS’nin myoklonik, atonik, atipik absans nöbetlerde dahi azalmaya neden olduğu gösterilmiştir (10).
Klas I | Nöbet sıklığında %80-100 azalma |
IA | İktal veya postiktal aktivitede gelişme var |
IB | İktal veya postiktal aktivitede gelişme yok |
Klas II | Nöbet sıklığında %50-79 azalma |
IIA | İktal veya postiktal aktivitede gelişme var |
IIB | İktal veya postiktal aktivitede gelişme yok |
Klas III | Nöbet sıklığında <%50 azalma |
IIIA | İktal veya postiktal aktivitede gelişme var |
IIIB | İktal veya postiktal aktivitede gelişme yok |
Klas IV | Yanlıca magnet ile fayda var |
Klas V | Gelişme yok |
Tablo 3: McHugh Sınıflaması
Etiyolojik açıdan değerlendirildiğinde ise idiyopatik olan olguların %50’sinde >%50 nöbet sıklığında azalma saptanmaktadır. En çok fayda göre grup ise post-travmatik epilepsi ve tuberoskleroz hastalarıdır (sırasıyla %78 ve %68). Epileptik ensefalopatilerde de etkinliği gösterilmiş ve hatta yalnızca düşme ataklarına değil ama birden fazla nöbet tipine etkin olması ve daha az invazif cerrahi gerektirmesi nedeniyle Lennox-Gastaut sendromunda kallozotomiden daha önce denenmesi gerektiğini belirten çalışmalar da bulunmaktadır (11-13).
Nöbet sıklığında azalma çalışmalarda birincil sonuç olarak değerlendirilmiştir, ancak bunun yanı sıra AEİ kullanımında azalma, yaşam kalitesine artış ve İED sıklığında azalma da ikincil sonuçlar olarak değerlendirilmiştir. Burada elde edilen şaşırtıcı sonuç, yaşam kalitesindeki artışın nöbet sıklığında azalmadan ve kullanılan AEİ sayısından bağımsız olduğudur. Hastaların bazılarında nöbet sıklığında azalma olmamasına rağmen veya belirgin bir azalma olmamasına rağmen yaşam kalitesinde artış saptanmıştır (14). VSS’nin pozitif bir psikotrop etkisi bulunmaktadır ki muhtemelen bunu mekanizma bölümünde de bahsedilen norepinefrin veya serotonin salınımındaki artışa borçludur. AEİ kullanımında azalma elbette olmakta ve genellikle yeni ilaç rejimi 2 yıl içerisinde yerleşmektedir. VSS bir ek tedavi olarak onay almış olmasına rağmen literatürde monoterapi olarak kullanılan ve 5 yıllık takibi bulunan bir olgu da sunulmuştur (15).
İnteriktal epileptiform deşarjlarda azalma nöbet sıklığının azalmasından bağımsız olarak saptanmıştır (16). İED’lerin sıklığı azalmış, kümeleşme eğilimi göstermiş ve yine bu kümelerin süresi de azalmıştır (17). Bunun yanı sıra uyanıklığın artması da ikincil bir etkidir. Özellikle serebral palsi hastalarında uyanıklığın artması sağlanarak yaşam kalitesinde belirgin artış sağlanmıştır (18).
Ülkemizde ise Sosyal Güvenlik Kurumunun 7 Eylül 2009 tarih ve B.13.2.SGK.0.11.00.00/769 sayılı genelgede belirtilen şartlar dahilinde VSS takılabilmektedir (19). Bu genelgeye göre VSS, sadece eğitim araştırma hastaneleri ve üniversite hastanelerinde uygulanması halinde; psikiyatri, nöroloji (çocuk/erişkin), beyin cerrahisi branşlarının birlikte bulunduğu heyet raporuna istinaden, kurumca bedeli karşılanır.
Vagal sinir stimülasyonunun uygulanma şartları: Hastanın yaşam kalitesini bozacak sıklık ve şekilde nöbetlerinin olması, nöbet tipine uygun bütün antiepileptikleri kullanmış olması ve halen en az 2’li (ikili) major antiepileptik ajanı 2 (iki) yıldır kullanıyor ve bunlara cevap alınamıyor olması, daha önce epileptik cerrahi uygulanıp yanıt alınamamış ya da epileptik cerrahi uygulanamaz durumda olması, epilepsi nedeninin malign beyin tümörü, nörometabolik ya da nörodejeneratif hastalık olmaması, hastaların zeka düzeyi ağır derecede geri olmamalı, hamile olmaması, sistemik kronik hastalık olmaması (Astım, Aktif Peptik Ülser, Kronik Akciğer Hastalığı, Koroner Kalp Hastalığı, Kronik Böbrek Hastalığı, Kronik Karaciğer Hastalığı, Diabetes Mellitus ve benzeri hastalıklar). Bunlara ek olarak 1. Uzun çekimli video-EEG kayıtları, 2. Hastanın daha önce kullandığı antiepileptik tedavi; doz, ilaç-kan seviyesi, nöbet sayısı ve şekli ile ilgili bilgilerin dökümante edildiği ayrıntılı epikriz (epikriz hasta takibini yapan nörolog ya da çocuk nörolog tarafından hazırlanmış ve imzalanmış olmalıdır), 3. Nöroradyolojik görüntüleme tetkiklerinin aslı ve 4. Psikolog tarafından düzenlenmiş zeka düzeyini gösteren belgenin değerlendirildiği nöroloji ve/veyaçocuk nörolojisi, beyin cerrahisi, psikiyatri uzmanından oluşan bir komisyon bulunmalıdır.
Sosyal güvenlik kurumunun ödeme planlaması ile ilgili olarak bazı kısıtlamalar getirmesi elbette anlaşılır bir uygulamadır ancak bunun bu yazıda özetlenen çalışmlaraın sonuçları ile uyumlu olmasını beklemek yanlış olmasa gerek. Görüldüğü gibi Türkiye’de hasta yaşı konusunda sınırlama bulunmamaktadır. Epilepsi cerrahisinden fayda görmemiş veya cerrahi adayı olmayan hastalara uygulama yapılması, majör AEİ’lerin denenmiş olması, nöbet sıklığının hayatı olumsuz etkileyecek düzeyde olması ise FDA kararı ile benzerlik göstermektedir. Yabancı literatürde belirtilmemekle birlikte malign neoplazma, nörodejeneratif veya nörometabolik gibi progresif seyirli olabilecek olgularda VSS kullanılmaması da bilimsel zeminde anlaşılır bir gerekçedir. Zeka düzeyinin değerlendirilmesi ve kronik hastalıklarda VSS uygulanmaması, bu grup hastalar arasında VSS’den fayda görebileceği düşünülen bazı olguların bu yöntemden mahrum kalması anlamına gelmektedir ki belki ileri dönemde bu kısıtlama kaldırılabilir.
Sonuç olarak, yaklaşık 2 dekattır 60000’den fazla hastaya uygulanan VSS’ne ait bilgiler oldukça sınırlıdır. Etki mekanizması net olarak bilinmemekte ve hipotetik cümleler ile ifade edilmektedir. FDA’nın sınırlamalarına rağmen tüm dünyada yapılan çalışma ve sunulan olgularda anlaşıldığı üzere uygulanan hastaların yaklaşık yarısında %50’den fazla nöbet sıklığında azalma görülmüştür. FDA’nın sınırlamasının aksine yalnızca parsiyel başlangıçlı epilepsi hastalarında değil jeneralize nöbeti bulunan hastalarda ve epileptik sendromlarda da oldukça etkin görünmektedir. 12 yaş sınırlaması büyük tenkit konusu olmaktadır. Ne kadar küçük yaşta uygulanırsa uzun dönemde o kadar fazla nöbet kontrolü sağlanmaktadır. Yapılan bu çalışmalardan elde edilen sonuçlar bir bütün olarak değerlendirildiğinde aşağıdaki şemada VSS uygulanabilecek hastaların nasıl seçileceği ve kullanılabilecek akış diyagramı sunulmuştur (Şekil 1) (20’den değiştirilerek). İlerleyen dönemlerde farklı sunumlarda konu ile ilgili uzmanların katkıları ile son halini alacağını düşündüğümüz bu akış diyagramı son halini almış bir öneriden ziyade bir ön hazırlık çalışması olarak değerlendirilmelidir. Oluşturulacak son diyagram ile birlikte sosyal güvenlik kurumunun ödeme planına ait şartları da belki ilgili uzmanlar tarafından tekrar değerlendirilebilecek konuma gelecektir.
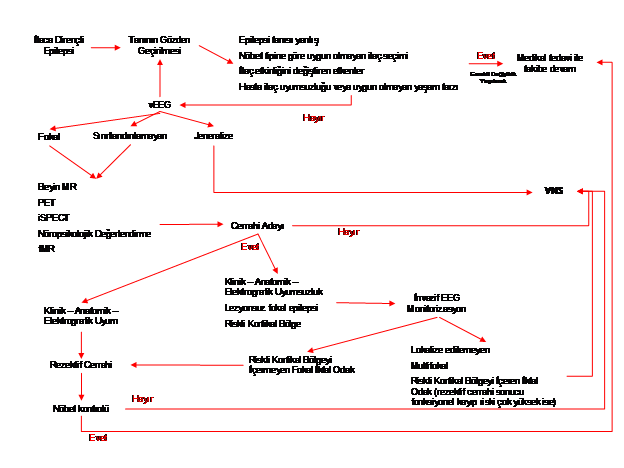
Şekil 1: VSS uygulanabilecek hastaların nasıl seçileceğine ilişkin akış diyagramı
KAYNAKÇA:
1. Penry JK, Dean JC. Prevention of intractable partial seizures by intermittent vagal stimulation in humans: preliminary results. Epilepsia. 1990;31 (sup 2): S40-S43.
2. Englot DJ, Chang EF, Auguste KI. Vagus nerve stimulation for epilepsy: a meta-analysis of efficacy and predictors of response. J Neurosurg. 2011; DOI: 10.3171/2011.7.JNS11977.
3. McHugh JC, Singh HW, Phillips J, Murphy K, Doherty CP, Delanty N. Outcome measurement after vagal nerve stimulation therapy: Proposal of a new classification. Epilepsia. 2007;48 (2): 375-378.
4. Elliot RE, Morsi A, Tanweer O, Grobelny B, Geller E, Carlson C, Devinsky O, Doyle WK. Efficacy of vagus nerve stimulation over time: Review of 65 consecutive patients with treatment-resistant epilepsy treated with VNS>10 years. Epilepsy Behav. 2011;20: 478-483.
5. Coykendall DS, Gauderer MWL, Blourin RR, Morales A. Vagus nerve stimulation for the management of seizures in children: an 8-year experience. J Pediatr Surg. 2010;45: 1479-1483.
6. Elliot RE, Rodgers SD, Bassani L, Morsi A, Geller EB, Carlson C, Devinsky O, Doyle WK. Vagus nerve stimulation for children with treatment-resistant epilepsy: a consecutive series of 141 cases. J Neurosurg Pediatr. 2011;7: 491-500.
7. Eliot, Morsi A, Kalhorn SP, Marcus J, Sellin J, Kang M, Silverberg A, Rivera E, Geller E, Carlson C, Devisky C, Doyle WK. Vagus nerve stimulation in 436 consecutive patients with treatment-resistant epilepsy: Long term outcomes and predictors of response. Epilepsy Behav. 2011;20: 57-63.
8. Burakgazi AZ, Burakgazi-Dalkilic E, Caputy AJ, Potolicchio SJ. The correlation between vagus nerve stimulation efficacy and partial onset epilepsies. J Clin Neurophysiol. 2011;28: 380-383.
9. Ghaemi K, Elsharkawy AE, Schulz R, Hoppe M, Polster T, Pannek H, Ebner A. Vagus nerve stimulation: Outcome and predictors of seizure freedom in long-term follow-up. Seizure. 2010;19: 264-268.
10. Rossignol E, Lortie A, Thomas T, Bouthiller A, Scarvarda D, Mercier C, Carmant L. Vagus nerve stimulation in pediatric epileptic syndromes. Seizure. 2009;18: 34-37.
11. Cersosimo RO, Bartuluchi M, DeLosantos C, Bonvehi I, Pomata H, Caraballo RH. Vagus nerve stimulation: effectiveness and tolerability in patients with epileptic encephalopathies. Childs Nerv Syst. 2011;27: 787-792.
12. You SJ, Kang HC, Ko TS, Kim HD, Yum MS, Hwang YS, Lee JK, Kim DS, Park SK. Comparison of corpus callosotomy and vagus nerve stimulatoin in children with Lennox-Gastaut syndrome. Brain Dev. 2008;30: 195-199.
13. Zamponi N, Passamonti, Cesaroni E, Trignani R, Rychlicki F. Effectiveness of vagal nerve stimulation (VNS) in patients with drop-attacks and different epileptic syndromes. Seizure. 2011;20: 468-474.
14. Vale FL, Ahmadian A, Youssef AS, Tatum WO, Benbadis SR. Long-term outcome of vagus nerve stimulation therapy after failed epilepsy surgery. Seizure. 2011;20: 244-248.
15. Rose S, Tao JX. Seizure freedom with VNS monotherapy: A case report. Seizure. 2011;20 (9): 735-737.
16. Mapstone TB. Vagus nerve stimulation: current concepts. Neurosurg Focus. 2008;25 (3): E).
17. Kuba R, Nesvadba D, Brazdil M, Oslejskova H, Ryzi M, Rektor I. Effect of chronic vagal nerve stimulation on interictal epileptiform discharges. Seizure. 2010;19: 352-355.
18. Jaseja H. Vagal nerve stimulation: Exploring its efficacy and success for an improved prognosis and quality of life in cerebral palsy patients. Clin Neurol Neurosurg. 2008;110: 755-762.
19. T.C. Sosyal Güvenlik Kurumu Genel Sağlık Sigortası Genel Müdürlüğü İlaç ve Tıbbi Malzeme Mevzuatı Daire Başkanlığının B.13.2.SGK.0.11.00.00/769 ve 07/09/2009 tarihli genelgesi.
20. Pati S, Alexopoulos A. Pharmacoresistant Epilepsy: From pathogenesis to current and emerging therapies. Cleve Clin J Med. 2010;77: 457-467
Bu yazıdaki bilgiler genel bilgi vermek amacı ile hazırlanmış olup bir doktordan alınan bilgilerin yerine kullanılamaz.
© Buradaki bilgilerin herhangi bölümü veya tamamı Prof. Dr Ersin Erdoğan’ın müsaadesi olmadan kullanılamaz veya çoğaltılamaz