Glial Tümörler ve Tedavisi
için Genel Bilgi
Gliomlar beyin ve omurilikte başlayan bir tür tümördür. Santral sinir sistenminde bulunan gliyal hücreler denilen destek hücrelerinden kaynaklandığı için Gliom olarak adlandırılır. Beyinde daha sık oranda görülmesi ile beraber serebellum ve omuriliktede görülebilir. Gliomları hücre tipine, histolojik özelliklerine derecesine (grade) ve lokalizasyonlarına göre sınıflandırmak mümkündür.
Hücre Tipine Göre
Gliomlar histolojik olarak belli hücre gruplarından kaynaklanırlar. Ana gliyoma hücre tipleri:
- Ependimomalar – Ependim Hücrelerinden kaynaklanırlar
- Astrositomalar – Astrosit denilen hücrelerden kaynaklanırlar en sık görülen glioblastomdur
- Oligodendrogliomalar – Oligodendrositlerden kaynaklanırlar
- Mikst giomalar– Bunlar birkaç değişik gliyal hücrenin bereber olduğu gliyal tümörlerdir örneğin oligoastrositomalar gibi.
Derecesine Göre
Gliomlar derecelerine göre kategorize edilirler bu şeklide tümörün patolojik tavrı hakkında bilgi sahibi olunur.
- Düşük Dereceli Tümörler: ( Dünya Sağlık Örgütü WHO grade II) bu tümörler benign olmamasına rağmen iyi prognoza sahiptirler
- Yüksek Dereceli Tümörler: (WHO Grade III-IV) bu gliomlar iyi diferansiye olmamış veya anaplastik olanlardır. Bu tümörler malign olup kötü prognoza sahiptirler.
En sık kullanılan derecelendirme sistemi WHO nun yaptığı sistemdir ve tümörler grade I den ( en iyi prognoza sahip) Grade IV e ( en kötü prognoza sahip olan) kadar derecelendirilirler.
Yerleşim Yerine Göre
Gliomlar serebrum ve serebellum arasındaki tentorium denilen her iki yapıyı birbirinden ayıran membranın altında (serebellum tarafı) veya üzerinde (serebrum tarafı) olmasına göre isimlendirilirler.
- Supratentorial: tentoriumun üzerinde serebrumda yerleşim gösterirler çoğunlukla erişkinlerde görülürler (% 70)
- İnfratentorial: tentoriumun altında serebellumda yerleşim gösterirler çoğunlukla çocuklarda görülürler (% 70)
- Pontin: beyin sapının pons kısmında yerleşim gösterirler: ponsun hayati öneme sahip fonksiyonları vardır
Hastaların Semptomları
Gliomaların semptomları hastalığın santral sinir sisteminin hangi bölümünü tuttuğuna bağlıdır. Beyin gliomları baş ağrısı, bulantı, kusma nöbet kranial sinir tutulumları ile kendini gösterir. Burada özellikle glioblastom gibi yüksek dereceli tümörlerin ileri düzeyde ödem oluşturacağı ve buna bağlı kafa içi basınç artışı bulguları verebileceği iyi bilinmeli nörolojik muayenede hastanın fundoskopisinde papil ödeminin varlığı hastada sabahları olan ve bazen kusma ile devam eden baş ağrılarının olabileceği bilinmelidir. Bazı optik gliom gibi lokalize tümörlerde görme kaybı ile kendini gösterir. Spinal kordta bulunan gliomlar ekstremitelerde ağrı uyuşma ve kuvvetsizlik ile kendini gösterirler. Gliomalar kan yolu ile yayılıp metastaz yapmazlar fakat Beyin Omurilik Sıvısı (BOS) ile yayılım yaparak drop metastaz denilen spinal korda yayılım gösterebilirler (özellikle epandimomlar).
Çocuklarda özellikle alt kranial sinir paralizilerinin eşlik ettiği subakut hastalıkla beraber uzun trakt bulguları (birinci motor nöron bulguları) bizlere pontin gliomlarını düşündürmelidir.
Patoloji
Yüksek dereceli gliomalar oldukça vasküler tümörler olup infiltre etme özelliği bulunur. Yaygın nekroz ve hipoksi alanları mevcuttur. Tümör sıklıkla kan beyin bariyerini yıkar ve bu sayede kontrast madde verildiğinde CT ve MRI da görülür hale gelir (şekil 1). Yüksek dereceli tümörler genellikle cerrahi olarak çıkarılsalar bile tekrarlarlar, bu nedenle bu tümörlere beyin kanseride denilir.
Diğer yandan düşük dereceli tümörler daha yavaş büyürler ve cerrahi olarak daha kontrol edilebilirler.
Gliomalarda yapılan genetik çalışmalar akkiz olarak olan birçok genetik mutasyonun olduğunu ortaya koymuştur. Tümör süpresyon 53 (P53) proteini erken mutasyonu vardır. P 53 için ‘genomun gardiyanı’ denilebilir, bunu yaparken hücre duplikasyonu esnasında DNA’nın tam kopyalanıp kopyalanmadığını kontrol eder ve bozuk kopyalandıysa yani mutasyona uğradıysa hücreyi yok eder (apoptozis). P53’ün kendisi mutasyona uğrarsa diğer mutasyonlar ve sonuçları durdurulamaz. Fosfataz ve tensin homolog denilen PTEN proteinide tehlikeli mutasyonlara sahip olan hücreleri yok eder. Epidermal büyüme faktör reseptörü denilen EGFR, bir büyüme faktörüdür ve hücrelerin bölünmesini ve çoğalmasını indükler. Bu ana proteinlerde oluşacak olan mutasyonlar hücrelerin kontrol dışı bölünmelerine neden olur. Buda kanserin ana belirleyicisidir. Son zamanlarda IDH1 ve IDH2 genlerinin belirleyici olduğu ortaya çıkarılmıştır, çünki bu genler mitokondrideki sitrat siklusunda önemli yer tutmaktadırlar. Mitokondinin apoptozisde önemli yeri vardır. Bundan başka bazı kanser hücrelerindeki glikoz metabolizmasındaki değişiklik hipokside bile glikozu parçalanabilir hale getirmektedir. Hipoksiye normal cevap olarakta yeni kan damarlarının büyümesinin stimülasyonuna neden olmaktadır (anjiogenezis). Sonuç olarak bu iki gen apoptozisin olmamasına ve gliomaların vaskülarizasyonunun artmasına sebep olamaktadır.
Prognoz
Gliomalar nadiren kürabldırlar. Yüksek dereceli gliomlarda prognoz özellikle de yaşlılarda genellikle kötüdür. Genel uluslararası verilerin Türkiye nüfusuna uyarladığımızda yılda ortalama 2000 – 2500 malign glioma olgusu teşhis edilmektedir. Bu hastaların yarısı biryıldan fazla %25’i ise iki yıldan fazla hayatta kalırlar. Anaplastik astrositomlarda ortalama sörvi üç yıl kadardır. Glioblastomlarda ortalama sörvi 12 ay kadar olup son tedavilerle 14 aya kadar artılmış ve 5 yıldan fazla yaşama oranları son tedavilerle istatistiksel anlamlı olarak artmıştır.
Düşük dereceli tümörlerde prognoz kesinlikle daha iyidir. Bir çalışma düşük dereceli oligodendrogliomlu hastalarda median sörvi 11.6 ay iken bir başka çalışmada 16.7 yıl olarak tespit edilmiştir.
Tedavi
Standart tedavi
Beyin gliomlarında tedavi lokalizasyona malignitenin derecesine göre değişebilmekle beraber sıklıkla kombine tedavi yaklaşımı uygulanır. Tedavinin en önemli ayağını cerrahi ve cerrahinin derecesi oluşturmaktadır, cerrahi hem patolojik tanının konulmasına hemde kanser hücrelerinin sayısının azalmasına ve daha sonraki tedavilerin etkinliğinin atrmasına sebep olmaktadır (Şekil 2a-b). Diğer tedaviler ise Radyoterapi ve kemotearpidir. Bu tümörlerde uygulanan radyoterapi genellikle eksternal beam radyoterapi şeklindedir. Nadir olgularda, küçük nüks veya rezidülerde stereotaksik radyocerrahide uygulanır. Son zanmanlarda uygulanan kemoterapotik ajan olan Temazolomide kan beyin bariyerini geçerek etkili olur.
Nükseden Malign Glial Tümörlerde Reoperasyon
Glioblastoma (GB)’nın gross total rezeksiyon (> %98) sonrasında yapılan radyoterapi + kemoterapi ile hastaların yaşam sürelerinde artış göstermesi ve yaşam kalitesinin arttığının ortaya konulması, klinik vaka serilerinde artan bir şekilde kendini göstermektedir. GB hastalarının % 10-30 unda reoperasyondan bahsedilmektedir. Literatürlerin çoğu prospektif non-randomize veya retrospektif olup mecburen değerlendirmeler bu yayınlarla yapılmaktadır.
Reoperasyonun Amacı
- Yaşam süresini uzatmak
- Yaşam kalitesini artırmak ve devam ettirmek
- Hastaların semptomlarını düzeltmek
- Yeni semptomların oluşumunu geciktirmek
- Kortikosteroid kullanımını azaltmak
- Kemoterapi ve radyoterapiye duyarlılığı artırmak ve intraoperatif kemoterapi uygulayabilmek
- Hastaya ilave defisit yaratmamak (cerrahi hastanın durumunu bozmamalı)
Tümör Rekürrensinde Görüntülemenin Yeri
Bilgisayarlı Tomografi (CT) ve Manyetik Rezonans Görüntüleme (MRI) tümör rekürrensini ortaya koymada sık olarak kullanılmaktadır. Gelecekteki karşılaştırmalarda hemen yapılmış olan postoperatif görüntülemeler faydalı olmaktadır. İlk 72 saatte yapılan MRI CT’den daha detaylı ve az artefaktlı bilgi vermektedir. Rutin aralıklı mı yoksa hasta semptomatik olduğunda mı görüntüleme yapılması hala tartışmalıdır. Bu tür hastalarda rekürrensin erken tespiti için hastaya yapılacak olan MRI sıklığı 2-3 ayda bir olmalıdır. Yapılan tedaviye yanıtın takibi için Macdonald kriterleri denilen kriterler olsa bile, tümör rekürrensi için ortak bir konsensüs yoktur. Buradaki zorluk, hastanın herhangi bir semptomu olmadan görüntülemelerde tedaviye bağlı olabilecek olan radyasyon nekrozu gibi değişikliklerin progresyon olarak yorumlanmasıdır, özellikle temozolomide kullanan hastaların %20 sinde pseudo-progresyon denilen görüntünün olduğu da akıldan çıkarılmamalıdır
Prognostik Faktörler
Cinsiyet
Cinsiyet ve sonuç arasında bir korelasyon yoktur.
Rekürrens Esnasındaki Yaş
Genç hastalar (≤ 40 yaş) yüksek performanslarını uzun süre sürdürürler. Yaşlı hastalar (> 60 yaş) reoperasyondan faydalanabilirler.
Performans Değerlendirilmesi
Genel olarak iki skor kullanılmaktadır; Karnofsky Performans Skoru (KPS) ve Avrupa kanser onkoloji grup (ECOG) skoru. KPS skoru ≥ 70 olan bir hasta kendine bakabilir fakat normal çalışmayı yapamaz bu ECOG skoru olarak 1 veya daha küçüğüne denk gelir. Yaşlı hastalardaki yapılan (> 60 yaş) reoperasyon ile reoperasyon yapılmamış olan genç hastaların sörvilerinin aynı olduğu gösterilmiştir. Semptomatik rekürrenli hastaların yapılan reoperasyon performans durumunda iyileşmeye neden olmuştur.
Rekürrens Şekli
Rekürrens genellikle primer tümör kenarlarının 2-3 cm içinde olmaktadır. Gidişatın kötü olduğu rekürrens derin ise, diğer tarafta ise, yaygın ise veya geniş bir yayılım söz konusu ise düşünülür. Bazı vaka serilerinde lokalizasyon ile sonuç arasında ilişki kurulamamıştır.
Reoperasyonun Zamanlaması
Reoperasyon için ideal zaman bilinmemektedir. Asemptomatik/orta derecede semptomatik olan hastalar semptomatik olanlara göre daha iyi yanıt verirler. İlk cerrahiden altı aydan daha uzun süre sonra rekürrens olması uzun yaşam ile doğru orantılıdır.
Cerrahi Prosedür
Mikrocerrahi prensipler beyin cerrahisinde standart hale gelmiştir ve tümör cerrahisinde de benzer prosedürler uygulanır. Rekürren GB daha agresif ve daha az sınırları belirgin olma eğilimindedir. Bu nedenle gross total (≥ %98) çıkarma daha zordur. Rezeksiyon sonrası yapılan radyoterapi ve kemoterapi ile oluşan gliozis nedeniyle pia tabakası daha az belirgindir. Bazı vaka serilerinde hassas alanların cerrahi için konturendikasyon oluşturmadığı belirtilmiştir. İntraoperatif MR ve/veya ultrason ve floresan işaretli tümör rezeksiyonu gibi intraoperatif görüntüleme teknikleri yardımcı olarak kullanılabilir. Multi-fokal, derin yerleşimli veya cerrahi olarak ulaşılması güç olan lezyonlarda radyo-nekrozu ekarte etmek için biyopsi yapılabilir. Onkolojik karar vermede rutin olarak tekrarlayan biyopsiler yapmanın faydası görülmemiştir.
Kaç Kez Reoperasyon Yapılabilir?
Bunun ile ilgili açık bir bilgi yoktur. Beş kez yapılan olgular rapor edilmiştir. Bir çalışma ilk ameliyattan sonraki yapılanların hastanın yaşam süresini uzatmadığını ifade etmektedir.
Reoperasyon ve Birlikte Yapılan Lokal Kemoterapi
Reoperasyon kemoterapi ile karşılaştırıldığında sonuçları daha iyidir. Reoperasyon intertisyal kemoterapi uygulanabilmesine olanak tanır. Bir randomize kontrollü çalışma cerrahi çıkarma ile cerrahi sonrası biodegradable carmustine emdirilmiş wafer (Gliadel®-MGI Pharma INC., USA) konulmasını karşılaştırmıştır. Çalışma ortalama dokuz hafta sörvide artış tespit etmiş ve 6 aylık mortalite oranları Gliadel® kullanılanlarda % 44 iken plasebo grubunda % 64’dür. Sistemik kemoterapiye bağlı yan etkiler bu hastalarda daha azdır.
Reoperasyonda Mortalite ve Morbitite
Mortalite oranları % 0 ila 11 arasında değişmektedir (genellikle % 5’in altında), morbitite ise % 13-69 arasındadır (%20).
Progresyon Tespit Edildikten Sonra Sörvi
Sörvi ile yaşam kalitesini (genellikle progresyonun olmadığı ve KPS nin 70 in üzerinde olduğu durumdur) birbirinden ayırt etmek çok önemlidir.
- Kontrol grubunda 1-2 ay
- Reoperasyondan sonra 3-13 ay
- “kabul edilebilen KPS’nun (KPS > 60) devam ettiği süre” 3-4 ay
Sonuç
Birçok çalışma adjuvan kemoterapi veya radyoterapi ile karşılaştırmış olmasına rağmen seçilmiş olgularda rekürren GB’larda reoperasyon artmış yaşam süre ve kalitesi ile doğru orantılıdır. Reoperasyon ortalama hayata 3 ila 5 ay katmaktadır. İdeal hasta 50 yaşından genç (ki yaşlı hastalar da faydalanmaktadır), KPS’u 60-70 den büyük veya eşit, tümörü iyi lokalizasyonda ki % 98 rezeksiyon yapılabilsin ve ilk ameliyat ile rekürrens arasında 6 aydan fazla zaman geçmesi gerekmektedir. Bu şartlar altında Gliadel implantasyonu, fokal radyoterapi veya radyocerrahinin de düşünülmesi uygun görülmektedir. Rekürren GB cerrahi tedavisi avantaj ve dezavantajları hasta ve ailesi ile tartışıldıktan sonra her zaman düşünülmelidir.
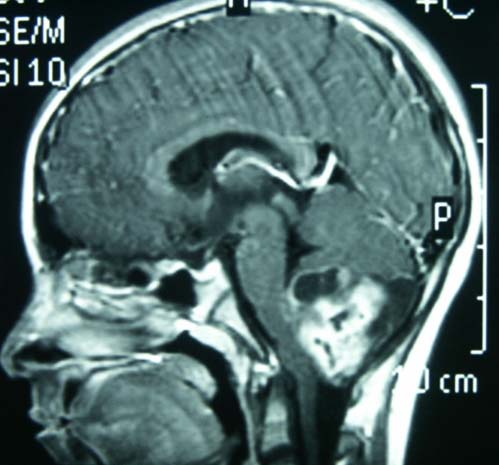
Şekil 1: Sagital kontrastlı T1 ağırlıklı MR görüntüsü infratentorial yerleşimli yoğun kontrast tutan pediatrik olgu
(Epandimom)
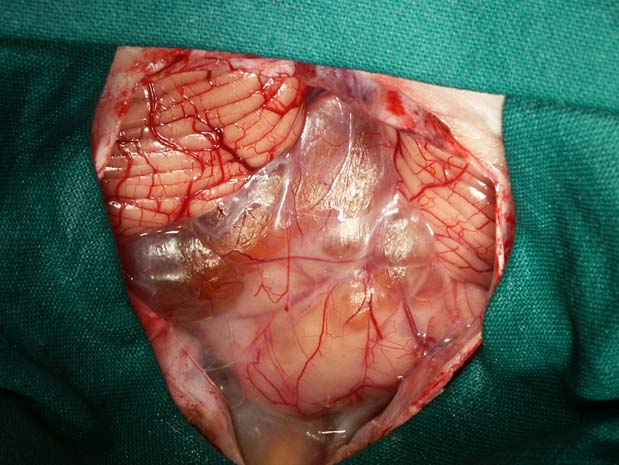
Şekil 2 a: Posterior fossa kraniotomisi yapılıp dura açıldıktan sonraki görüntü.(daha önceki MR görüntüsi olan olgu, şekil 1) Serebellum tümör tarafından yukarı itilmiş olarak görülmekte
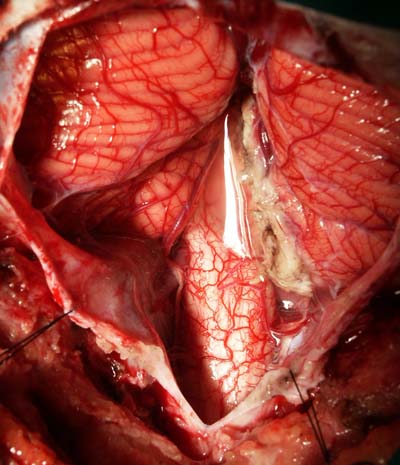
Şekil 2 b: Tümör total olarak çıkarıldıktan sonraki normal anatomik görüntü.
Bu yazıdaki bilgiler genel bilgi vermek amacı ile hazırlanmış olup bir doktordan alınan bilgilerin yerine kullanılamaz.
© Buradaki bilgilerin herhangi bölümü veya tamamı Prof. Dr Ersin Erdoğan’ın müsaadesi olmadan kullanılamaz veya çoğaltılamaz