Giriş
Hem birincil hem de ikincil Santral sinir sistemi lenfoması, non-Hodgkin lenfomanın nadir bir alt kümesini temsil eder. Dünya Sağlık Örgütü tanımına göre, birincil merkezi sinir sistemi lenfoması, SSS (Santral Sinir Sistemi) parankiması, dura, leptomeninksler, kranial sinirler ve omurilik veya immün yetmezlikli hastalarda göz içi kompartımanı ile sınırlı olan vakaları ifade eder. Öte yandan, sekonder SSS lenfoması, SSS’ne yayılmış sistemik non-Hodgkin lenfoma anlamına gelir. Tarihsel olarak, birincil santral sinir sistemi lenfomalarının prognozu, tedavi edilmediğinde 1,5 aylık genel sağkalım ve %30'luk beş (5) yıllık sağkalım oranı ile çok iç karartıcı olmuştur. Bu arada, agresif sistemik non-Hodgkin lenfoma hastalarının sekonder SSS hastalığı geliştirme riski %2 ila 27'dir ve tanıdan sonra medyan sağkalım 2,2 aydır. Yüksek doz metotreksat bazlı kemoterapi rejimlerinin kullanıma girmesi nedeniyle, SSS lenfomaları olan hastaların tedavisinde önemli ilerlemeler kaydedilmiştir ve bu da hayatta kalma oranlarının artmasına yol açmaktadır.
Etiyoloji
Hem birincil hem de kazanılmış immün yetmezlik, merkezi sinir sistemi lenfoması için önemli bir risk faktörüdür. Primer SSS lenfoması, AIDS'li hastaların yaklaşık %6'sında görülür ve AIDS'i tanımlayan bir hastalıktır. Genellikle CD4 sayıları çok düşük olduğunda, sıklıkla antiretroviral tedavi almayan hastalarda ortaya çıkar. Bu arada, kalp, karaciğer ve akciğer nakli hastalarının %2 ila 7'si ve böbrek nakli hastalarının %2'ye varan oranı nihayetinde hastalığa yakalanır. İnsidans, kalp ve akciğer nakli sonrası ilk yılda en yüksektir. Wiskott Aldrich, ataksi telanjiektazi, ortak değişken ve şiddetli kombine immün yetmezlik sendromları gibi primer immün yetmezlik, primer merkezi sinir sistemi lenfoması gelişme riskini %4 verir. Epstein bar virüsü (EBV), organ nakli sonrası immünosüpresanlar alan hastalar gibi T hücresi immün yetmezlikli durumlarda SSS lenfoma ile yüksek oranda ilişkilidir. EBV ayrıca AIDS'li hastalardaki primer SSS lenfomalarının %100'ü ile ilişkilidir.
Epidemiyoloji
Primer SSS lenfoma, Amerika Birleşik Devletleri'nde yıllık yaklaşık 1400 vaka insidansına sahiptir. Tüm primer beyin tümörlerinin %5'ini ve tüm non-Hodgkin lenfoma vakalarının %1'ini oluşturur. Oldukça aktif antiretroviral tedavinin (HAART) ortaya çıkması nedeniyle AIDS popülasyonunda SSS lenfoma azalırken, yaşlı popülasyonda insidansı artmaktadır. Oranlar, yaşlılar ve bağışıklık sistemi zayıf olan kişilerde en yüksektir, ancak pediatrik popülasyonda hastalık nadirdir. Bağışıklığı yetersiz hastalara genellikle 50 ila 70 yaşları arasında teşhis konurken, bağışıklığı baskılanmış hastalar 30'lu ve 40'lı yaşlarında daha erken başvururlar. [4]Erkekler, her iki grupta da kadınlardan daha sık etkilenir, ancak nakil sonrası lenfoproliferatif SSS lenfomalı hastalarda SSS lenfoma için cinsiyet ayrımı yoktur.
Patofizyoloji
Primer santral sinir sistemi lenfomalarının en sık tutulan bölgeleri, beyin sapı, serebellum ve omurilik daha az etkilenen frontal lob ve bazal ganglionlardır. Primer santral sinir sistemi lenfoması olan hastaların %25'e varan bir kısmında göz içi lenfoma gelişir ve primer göz içi lenfoma sonuçta zamanın %80'inden fazlası SSS'ne yayılır. Primer intraoküler lenfoma lezyonları vitreus sıvısı ve retinada daha sık bulunma eğilimindedir. Bununla birlikte, primer SSS lenfomanın sistemik olarak yayılması nadirdir. Öte yandan, SSS'nin sekonder lenfoması sıklıkla dura ve leptomeninksleri ve intraoküler tutulum durumlarında koroidi tercih eder.
B hücresi aktivasyonu, farklılaşması ve apoptozda yer alan tümör baskılayıcı ve proto- onkogenlerdeki birkaç mutasyonun, birincil SSS lenfoma gelişimine katkıda bulunduğuna inanılmaktadır. Primer SSS lenfoma vakalarında MYC, PAX5, Rho/TTF ve PIM1 gibi proto- onkogenlerde ve ayrıca PRDM1 gibi tümör baskılayıcı genlerde somatik hipermutasyonlar gösterilmiştir. NF-KB sinyalinin hastalık patogenezinde rol oynadığına inanılmaktadır. MYD88, CADR11 ve CD79 gibi NF-KB yolu içindeki aktivatörlerin yukarı regülasyonu ve ayrıca TNFAIP3 gibi NF-KB inhibitörlerinin baskılanması, birincil SSS lenfomalı bireylerde ortaya çıkmıştır. Sekonder SSS lenfomasında MYD88 ve CD79B mutasyonlarının ekspresyonu, primer SSS lenfomasına göre oldukça düşüktür ve bu da farklı patogenezi düşündürür. JAK/STAT yolağının anormal düzenlemesi de söz konusudur. Primer SSS lenfoma hastalarının BOS analizinde artan IL-10 seviyeleri, A JAK/STAT aracısı görülür ve sıklıkla daha kötü bir prognoz ile ilişkilendirilir. Primer SSS lenfoma hücrelerinin ilk olarak SSS'nin içinden mi ortaya çıktığı, yoksa sistemik olarak daha sonra periferik kan yoluyla SSS'ye gidip başka mutasyonları biriktirip biriktirmediği hala açık değildir.
Histopatoloji
Primer SSS lenfomalarının yaklaşık %95'i diffüz büyük B hücre (DLBC) kategorisine aittir ve geri kalanı düşük dereceli B hücreli lenfoma, T hücreli lenfoma ve Burkitt lenfomadır. Diffüz büyük B hücreli lenfomanın iki histolojik varyantı vardır: germinal merkez alt tipi, genellikle CD10 ve BCL6 pozitif ve genellikle MUM1'i eksprese eden aktif B hücresi alt tipi. Primer SSS lenfomalarının yarısından fazlası hem BCL6 hem de MUM1'i eksprese eder, bu da tümörün germinal merkezden çıkma sürecindeki B hücrelerinden türediğini ancak bunun henüz post germinal merkez aşamasına ulaşmadığını düşündürür. Primer SSS lenfomaları genellikle pan B hücre belirteçleri CD19, CD20, CD22 ve CD79a'yı ifade ederken, plazma hücre belirteçleri CD38 ve CD138 genellikle yoktur. Vakaların sadece %10'u CD10 pozitiftir, ancak tümörlerin %80-90'ı MUM1 pozitiftir ve %60-80'i BCL6 pozitiftir. Bu B hücresi farklılaşma belirteçlerinin prognostik değeri, sistemik diffüz büyük B hücreli lenfomalarda iyi açıklanmış olsa da, primer SSS lenfomadaki önemi belirsizliğini koruyor. Benzer şekilde, hücre döngüsü düzenleyici protein MYC'nin ve ayrıca anti-apoptoz proteini BCL2'nin aşırı ekspresyonunun, sistemik DLBC lenfomada prognostik etkileri vardır, ancak primer SSS lenfomalarında belirsiz bir önemi vardır.
Primer SSS lenfoması oldukça hücresel ve infiltratif bir tümördür. Hücreler genellikle anjiyotropizm adı verilen ve daha kötü bir prognoz ile ilişkili olduğu gösterilen perivasküler bir büyüme modeli sergiler. Diffüz büyük B hücreli lenfomanın lenfomatozis serebri varyantı nadiren görülür. Mevcut olduğunda T hücrelerinin reaktif perivasküler infiltratı daha iyi bir sonuç ile ilişkilidir. Bu antitümör T hücresi immün yanıtı, sistemik DLBC lenfomaları ile karşılaştırıldığında primer SSS lenfomalarında daha az görülür ve bu, kısmen daha kötü prognozunu açıklayabilir.
Klinik
Primer CNS lenfomalı hastaların %80'e kadarında fokal nörolojik defisit vardır ve semptomlar genellikle lezyonun yeri ile ilişkilidir. Hastaların %32 ila %43'ünde davranışsal ve zihinsel durum değişiklikleri ve hastaların %32 ila %33'ünde artmış kafa içi basınç belirtileri mevcuttur. Nöbetler nadirdir ve hastaların sadece %11 ila %14'ünde görülür. Sistemik lenfomanın merkezi sinir sistemi tutulumu genellikle hastalığın erken evrelerinde, sistemik hastalığın teşhisinden ortalama 5 ila 12 ay sonra ortaya çıkar. Hastalar sıklıkla baş ağrısının yanı sıra leptomeningeal metastazlardan kaynaklanan kraniyal veya spinal nöropati ile başvururlar. Göz içi lenfoma genellikle ağrı, görme keskinliğinde azalma, fotofobi, bulanık görme ve uçuşan cisimler ile kendini gösterir. Semptomlar steroid uygulamasıyla hızla iyileşirken, steroidler sıklıkla yanlış negatif biyopsilerle sonuçlanır, bu nedenle kesin tanı konulana kadar kullanımı uygun değildir.
Değerlendirme
Primer santarl sinir sistemi lenfoması şüphesi olan hastalarda, tanıda kontrastlı beyin MRG önerilen ilk testtir. Lezyonlar sıklıkla periventriküler bölgede olduğu kadar serebral beyaz cevherde merkezi olarak yerleşir. Kontrastsız T1 ağırlıklı görüntülemede sıklıkla izointens veya hipointens ve T2'de izointens veya hiperintenstirler. BT, MRG kadar hassas değildir, ancak genellikle kontrast sonrası kontrastlanma ile birlikte izo veya hiperatenüe lezyonlar gösterir. İmmün yetmezlikli hastalardaki lezyonlar genellikle homojen tutulumla soliter iken, vakaların %20 ila %40'ında çoklu lezyonlar rapor edilir ve vakaların %13'e kadarında halka benzeri kontrastlanma meydana gelir. Çevreleyen ödem genellikle mevcuttur, ancak malign gliomalarda veya metastatik hastalıkta görülen ölçüde değildir. Bunlara ek olarak, perivasküler boşluk boyunca lineer artış, birincil santral sinir sistemi lenfoması ile yüksek oranda ilişkilidir. Buna karşılık, immün yetmezlikli hastaların %30 ila %80'i, genellikle nekroza sahip olan ve kontrast sonrası düzensiz bir halka kontrastlanma paterni ile sonuçlanan çoklu lezyonlarla başvurur. Primer SSS lenfomanın primer dural alt tipinde, diffüz kontrastlanan kitleler genellikle BT ve MRI'de görülebilir ve bir menenjiyomu taklit edebilir. Yüksek dereceli gliomalarda mikro kanamalar sıklıkla bulunurken, kanama ve kalsifikasyonlar, AIDS ile ilişkili vakalar dışında primer SSS lenfoma lezyonlarında nadirdir.
Konvansiyonel manyetik rezonans görüntüleme tek başına SSS lenfomasını beyindeki diğer neoplastik lezyonlardan güvenilir bir şekilde ayırt edemez, bu nedenle diğer sekanslar ve görüntüleme modaliteleri genellikle yardımcı olur. Primer santral sinir sistemi lenfomaları, difüzyon ağırlıklı MRG sekanslarında onları metastazlar ve yüksek dereceli gliomalardan daha hiperintens yapan oldukça hücresel tümörlerdir. Karşılık gelen görünen difüzyon katsayısı (ADC) değerleri de daha düşüktür ve genel sağkalımı öngörebilir. Bununla birlikte, AIDS'lilerle ilişkili SSS lenfomaları, serebral toksoplazmoz ile karşılaştırıldığında benzer şekilde düşük ADC değerlerine sahiptir ve yalnızca ADC değerlerine dayalı olarak güvenilir bir şekilde ayırt edilemez. Bu durumda, MR spektroskopisi, lenfoma ve toksoplazmozun farklı biyokimyasal özelliklere sahip olması nedeniyle bazı faydalar sağlayabilir.
Ek olarak, SSS lenfomaları genellikle gliomalardan daha hipermetaboliktir, bu da metiyonin PET ve FDG PET taramaları gibi metabolik görüntülemede alımın artmasına neden olur. PET görüntülemedeki alım alanı genellikle geleneksel görüntülemedeki karşılık gelen alanlardan daha geniştir, bu da tümörün MR görüntülemede gösterilen alanların ötesine infiltrasyonunu yansıtır. Öte yandan, enfeksiyöz lezyonlar genellikle hipometaboliktir ve SPECT ve SPET'te daha düşük talyum-201 alımına ve PET görüntülemede daha düşük FDG alımına karşılık gelir. Bu, bağışıklığı baskılanmış bireylerde birincil santral sinir sistemi lenfomalarının enfeksiyöz etiyolojilerden ayırt edilmesine yardımcı olur.
MRG'nin intraoküler lenfomayı tespit etme hassasiyeti düşüktür, bu nedenle makula veya uvea üzerinde nodüler kontrast oluşturan lezyonları ortaya çıkarmak için ince bir kesit protokolü gerekir. Primer vitreoretinal lenfomanın kesin tanısı için tercih edilen yöntem vitreus aspirasyonu veya korioretinal biyopsi olmakla birlikte, her iki gözün de yarık lamba muayenesi genellikle çalışma sürecinde daha erken yapılır. Flow sitometri, primer dural lenfoma, posterior fossa lezyonları veya sekonder SSS lenfoması durumlarında BOS analizinin yanı sıra vitreus aspirat analizinde kullanılabilir. Nihayetinde, stereotaktik iğne biyopsisi, özellikle oküler veya BOS tutulumu olmayan hastalarda intraparankimal lezyonların kesin tanısına izin verir.
Tedavi / Yönetim
Radyasyona karşı yüksek duyarlılığı nedeniyle, yeni teşhis edilmiş merkezi sinir sistemi lenfomaları olan hastalar geleneksel olarak tüm beyin radyoterapisi (WBRT) ile tedavi görmektedir. İlk yanıtlar yüksek olmakla birlikte, hayatta kalanlar arasında erken nüks ve radyasyonla ilişkili nörotoksisite yaygındı. Ayrıca, WBRT tek tedavi olduğunda medyan genel sağkalım 12 ila 18 aydı. 1970'lerde yüksek doz metotreksat (HD-MTX) kemoterapi rejimlerinin kullanılmaya başlanmasıyla birlikte, SSS lenfomalı bireylerde daha iyi sağkalım meydana geldi. Tek tedavi olarak kullanıldığında, yüksek doz metotreksat ile ortalama genel sağkalım 25 ila 55 aydı.Primer SSS Lenfomasının cerrahi rezeksiyonu belirgin bir fayda göstermemiiştir. Primer SSS Lenfomasında cerrahinin rolü, histopatolojik tanıyı koymak için biyopsi ile sınırlıdır.
Şu anda, CNS lenfomalı bireyler için tedavinin temel dayanağı, tam bir radyografik yanıtı (CR) amaçlayan indüksiyon kemoterapisi ve ardından konsolidatif tedavidir. Konsolidatif tedavinin amacı, rezidüel hastalığı ortadan kaldırmak ve genel sağkalımı iyileştirmektir. İndüksiyon kemoterapisi genellikle yüksek doz metotreksatın (HD-MTX) temozolomid, sitarabin, etoposid, vinkristin, karmustin, ifosfamid, tiotepa ve siklofosfamid gibi diğer kemoterapi ajanlarıyla bir kombinasyonunu içerir. Konsolidasyon seçenekleri arasında yüksek doz radyasyon (45 Gy), düşük doz radyasyon (23.4 Gy) ve karmustin, tiotepa, siklofosfamid, busulfan, sitarabin ve etoposid gibi ajanlarla yoğun doz kemoterapi yer alır. Birleştirici tedavi olarak azaltılmış doz WBRT ile yapılan çalışmalar, iyi progresyonsuz ve genel sağkalım oranları göstermiş olsa da, radyasyonun uzun vadeli nöropsikolojik etkilerini belirlemek için daha uzun bir takip süresi gereklidir. Daha da önemlisi, WBRT'yi konsolidatif tedaviden çıkaran çalışmalarda, hayatta kalma konusunda herhangi bir uzlaşma gösterilmedi ve hastaların daha iyi bir nörolojik sonucu vardı.
Bir çalışmada, indüksiyon için HD-MTX'e sitarabin, ardından konsolidasyon için WBRT eklendi ve 3 yıllık genel sağkalım %46 iken, HD-MTX monoterapisiyle %32 idi. Bir başkasında, indüksiyon sırasında HD-MTX'e tiotepa ve rituximab, ardından konsolidasyon için WBRT eklendi ve genel sağkalım, yalnızca HD-MTX ile %42'ye karşı %69 idi. İndüksiyon için prokarbazin, vinkristin ve rituximab ile birlikte HD-MTX, ardından sitarabin ve azaltılmış doz konsolidatif radyoterapi kullanıldığında, indüksiyona tam yanıt (CR) elde eden hastalarda 3 yıllık genel sağkalım oranı %87 idi. Ayrıca, medyan genel sağ kalıma 6 yılda ulaşılmadı CALGB 50202 denemesi, HD-MTX'in indüksiyon için oral temozolomid ve rituksimab (MT-R) ve ardından konsolidasyon için etoposid ve sitarabin (EA) ile kullanımını araştırdı. Hastaların %66'sı indüksiyon tedavisine (CR) tam yanıt verdi ve iki yılda progresyonsuz sağkalım oranı 0,57 idi Benzer şekilde, 5 yıllık takipte medyan genel sağkalıma ulaşılmadı.
Miyeloablatif tedavi ve otolog kök hücre nakli de konsolidasyon için seçeneklerdir. Bir çalışmada indüksiyon için sitarabin, tiotepa ve rituximab ile birlikte HD-MTX'i, otolog kök hücre nakli ile yüksek doz karmustin ve tiotepa ile miyeloablatif tedavi izledi. 2 yılda genel sağkalım oranı %87 idi. Benzer bir çalışmada, HD-MTX bazlı bir indüksiyon rejiminden sonra, tiotepa, busulfan ve siklofosfamid ile şartlandırma tedavisi ve ardından kök hücre nakli sağlandı. 2 yıllık genel sağkalım oranı %81 ve progresyonsuz sağkalım oranı %79 idi. 10 yılda, benzer bir çalışmada genel sağkalım oranı %35 idi, bu da bunun özellikle genç hastalar için etkili bir konsolidasyon seçeneği olabileceğini düşündürmektedir CALGB 51101, CALGB 50202 çalışmasının başarılarına dayanarak başlatıldı ve şu anda etoposid ve sitarabin ile konsolidatif tedaviye karşı karmustin ve tiotepa ile miyeloablatif tedaviye karşı, ardından yüksek doz metotreksat, temozolomid ve rituximab (MT-R) sonrasında kök hücre nakli araştırılıyor.
Ne yazık ki, SSS lenfomalı hastaların çoğunda nüks 5 yıl içinde görülse de ilk tedaviden 10 yıl sonrasına kadar nükslerin görülmesi nadir değildir. Optimal kurtarma rejimi araştırma aşamasındayken, tiotepa, sitarabin, sitarabin lipozom enjeksiyonu, etoposid ve ifosfamid gibi diğer santral sinir sistemi penetrantları ile birlikte daha önce duyarlıysa ek HD-MTX umut verici sonuçlar göstermiştir. Ek olarak, miyeloablatif tedavi ve ardından kök hücre nakli genç hastalarda iyi bir seçenektir. Daha önce kullanılmadıysa, WBRT, 11 ila 19 aylık medyan genel sağkalım oranıyla etkili bir kurtarma seçeneği olmaya devam ediyor. [1]Lenalidomid, ibrutinib, buparlisib, nivolumab, pemetrexed, pomalidomid, temsirolimus ve pembrolizumab gibi birkaç yeni terapötik ajan şu anda araştırılmaktadır.
Göz içi lenfoma tedavisi için bir çalışma, HD-MTX ve rituximab bazlı indüksiyonu, ardından sitarabin ve etoposid ile konsolidasyonu önermiştir. Göz içi lenfoma ayrıca binoküler dış ışın radyasyonuna da iyi yanıt verir. Tek taraflı hastalıkta intravitreal rituksimab ve MTX etkili bir seçenek olmaya devam etmektedir. Ancak, nöraksis içinde başka bir yerde hastalıktan şüpheleniliyorsa, sistemik kemoterapi yeniden önerilir.
Yüksek riskli sistemik non-Hodgkin lenfoma hastalarında CNS yayılmasını önlemek için HD- MTX ile profilaksi düşünülebilir. Bu hastalardaki yüksek riskli özellikler, yüksek bir uluslararası prognostik indeks skoru ve özellikle testislerde olmak üzere ekstranodal hastalığın varlığını içerir.
Ayırıcı tanı
Santral sinir sistemi lenfomalarının ayırıcı tanısı geniştir. Yüksek dereceli gliomalar, menenjiyom, granülomatöz ve demiyelinizan hastalıklar ve ayrıca vaskülit dikkate alınmalıdır. Sistemik malignitelerden kaynaklanan metastatik hastalık ve nöraksis içindeki enfeksiyonlar da benzer şekilde ortaya çıkabilir ve dikkatli bir öykü ve tanısal inceleme ile ekarte edilmelidir. Ek olarak, serebral toksoplazmoz gibi enfeksiyöz etiyolojiler, özellikle AIDS'ler gibi bağışıklık sistemi baskılanmış hastalarda olasılıklar olarak değerlendirilmelidir.
Toksisite ve Yan Etki Yönetimi
Hastaların %5 kadarında yüksek doz metotreksat kullanımına bağlı nefropati gelişir. Yeterli hidrasyon, idrar alkalileştirme, penisilin ve metotreksat ile etkileşime giren diğer ilaçlardan kaçınma, bu toksisiteyi azaltmanın yollarıdır. Öneriler, görüntüleme için iyotlu kontrast kullanımı ile yüksek doz metotreksat uygulaması arasında iki günlük bir boşluk bırakılmasıdır. Yükseltilmiş dozlama stratejileri ile lökovorin kurtarma ve böbrekler yoluyla metotreksat klirensini kolaylaştırmak için karboksipeptidaz G2 enziminin kullanımı da etkili seçeneklerdir.
Evrelendirme
Başlangıçta primer SSS lenfoması olduğu düşünülen hastaların yaklaşık %4 ila %12'sinin sistemik hastalığa sahip olduğu bulunmuştur. Evreleme sürecinde omurga MRG, göğüs BT, karın ve pelvis, kemik iliği biyopsisi, PET görüntüleme ve seçilmiş vakalarda testis ultrasonu yapılabilir. PET görüntüleme, sistemik hastalığı saptamada konvansiyonel BT göğüs, karın ve pelvise göre daha duyarlı olabilir ve kemik iliği biyopsisi, evreleme sürecinde diğer görüntüleme modalitelerinde belirgin olmayan hastalığı saptayabilir. LDH, HIV ve hepatit B ve C serolojisinin temel seviyeleri sıklıkla yapılır. Ayrıca SSS lenfomalı hastaların %15-25'inde göz içi tutulum da olduğundan, oftalmolojik yarık lamba muayenesi standarttır. İntraoküler lenfoma tanısı alan hastalarda BOS değerlendirmesiyle birlikte kontrastlı beyin MRG'si de alınmalıdır, çünkü bu hastaların %80'inde sonuçta merkezi sinir sisteminin diğer bölgelerinde lenfoma gelişir. Optik koherens tomografi ve floresan anjiyografi de intraoküler lenfoma tanı ve evrelemesinde seçenekler olabilir.
Prognoz
Tedavi edilmemiş primer SSS lenfoma için genel sağkalım yaklaşık 1.5 aydır. Serum laktat dehidrogenaz seviyeleri, Eastern Cooperative Oncology Group (ECOG) skoru 1'den büyük, yaş 60'tan büyük, BOS protein seviyesi ve erişimi zor olan derin beyin yapılarında lezyonların varlığı dahil olmak üzere çeşitli değişkenlerin prognozla ilişkili olduğu bilinmektedir. Geçmişte yaş tekrarlanabilir bir prognostik indeks iken, daha yeni çalışmalar prognoz ile yaş arasındaki ilişkinin tedaviye bağlı olduğunu göstermiştir. Primer SSS lenfoma, diğer primer beyin tümörleriyle karşılaştırıldığında genellikle kemoterapi ve radyasyona daha olumlu bir yanıt verir, ancak nüks eden hastalarda prognoz kötü olabilir. Düşük dereceli B hücreli lenfomalar daha olumlu uzun vadeli sonuçlara sahipken, T hücreli lenfomalar ve intravasküler büyük B hücreli lenfomalar genellikle çok agresiftir ve kemo-radyasyon tedavisine zayıf yanıt verir. SSS lenfomalarında yüksek doz metotreksat kullanımının prognozu iyileştirdiği güvenilir bir şekilde gösterilmiştir.
Komplikasyonlar
WBRT ile tedavi edilen hastalarda yürüme bozuklukları, hafıza kayıpları ve idrar kaçırma gibi çeşitli nöropsikolojik komplikasyonlar ortaya çıkabilir. Bunlar en sık 60 yaşından büyük kişilerde görülür. Tedavi sonrası bireylerde travma sonrası stres bozukluklarına ilişkin raporlar da mevcuttur. İkinci malignite gelişme riski, özellikle genç yaş gruplarında, uzun süreli SSS lenfoma sağ kalanlarında artar. Sekonder SSS lenfoması olan hastalar, göğse radyasyon uygularlarsa, radyasyonla ilişkili kardiyovasküler hastalık riski artacaktır. Doksorubisin gibi antrasiklinlerin kullanımı kardiyotoksisite göstermiştir ve rituximab kullanımı ilerleyici multifokal lökoensefalopati riskinde artış göstermiştir. Nakil sonrası SSS lenfoma hastalarında, özellikle bağışıklık fonksiyonunu yeniden oluşturmak için bağışıklık bastırıcı azalırsa veya durursa, allogreft başarısızlığı bir risktir.
Hasta Eğitimi
Hastalar, hastalık süreçleri ve tedavi görürken kaçınılması gereken olası tuzaklar hakkında eğitime ihtiyaç duyarlar. Metotreksat, yüksek dozlarda verildiğinde renal tübüllerde çökelebilir ve doğrudan tübüler hasara neden olabilir. Bu risk, idrar çıkışı azalmış durumlarda ve ayrıca asidik idrarda artar. Yeterli hidrasyon çok önemlidir. Ayrıca, NSAID'ler, penisilinler, probenesid, fenitoin, siprofloksasin, proton pompası inhibitörleri ve levetirasetam gibi bazı ilaçlar metotreksatın renal klirensini etkiler ve bu nedenle mümkün olduğunda kaçınılmalıdır.
Santral sinir sistemi lenfomalarının başarılı tedavisi, tedavi öncesinde, sırasında ve sonrasında hastanın yaşam kalitesini artırmak için işbirlikçi ve meslekler arası bir ekip yaklaşımı gerektirir; bu genellikle aşağıdakiler gibi çeşitli alt uzmanlık alanlarındaki uzmanlardan oluşan bir ekibi içerir:
Tıbbi onkologlar
nörologlar
nöroradyologlar
Algoloji uzmanları Fiziksel ve mesleki terapistler psikiyatristler
Beyin cerrahları, nöropatologlar, radyasyon onkologları, göz doktoru
Sosyal çalışanlar
Onkoloji hemşireleri Palyatif bakım uzmanları
Yukarıda sıralananlara ek olarak hemşirelik ve eczacılık, SSS lenfomanın yönetiminde çok önemli roller oynayacaktır. Hemşirelik, daha önce tartışıldığı gibi birçoğu daha sonra terapötik sonuçlar verebilecek olan ilaç-ilaç etkileşimlerine karşı kontrol ederken ajan seçimlerini ve tüm dozları doğrulayacak bir onkoloji uzmanı eczacının girdisi olması gereken kemoterapiyi uygulayacaktır. Hemşire, terapötik etkinliği not etmenin yanı sıra aksi reaksiyonlara karşı uyanık olmalı ve herhangi bir problemi recete eden doktora bildirmelidir. Bu şekilde, tüm bu çeşitli disiplinler, sonuçları optimize etmek için hastalık yönetimine yönelik işbirlikçi meslekler arası ekip yaklaşımına katkıda bulunabilir. [Seviye V]
SSS lenfomanın korumalı bir prognozu vardır; her tedavinin morbiditeye katkıda bulunan önemli yan etkileri vardır. Tedaviye yanıt veren hastalarda bile nüks yaygındır. Acımasız prognoz nedeniyle, palyatif bir ekibin bu hastaların bakımına erkenden dahil olması gerekir. Prognozu değiştirmeyen kapsamlı testler ve prosedürlerle konforlu bakım ve yaşam kalitesinden ödün verilmemelidir.
SSS Primer lenfomanın MR Görüntüsü (kendi olgularımızdan bir örnek)
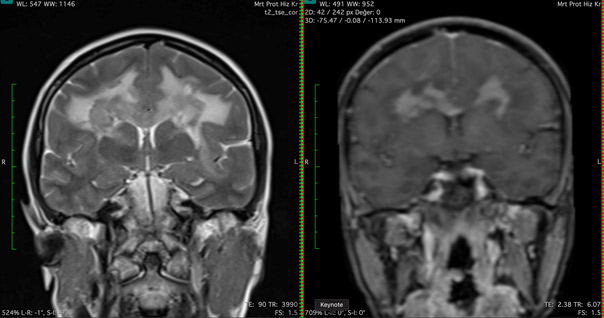
Kaynak: Keva Green; Jeffery P. Central Nervous System Lymphoma
Hogg StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022 Jan-.